Calore latente di fusione
Calore latente di fusione
Questo sito utilizza cookie, anche di terze parti. Se vuoi saperne di più leggi la nostra Cookie Policy. Scorrendo questa pagina o cliccando qualunque suo elemento acconsenti all’uso dei cookie.I testi seguenti sono di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente a studenti , docenti e agli utenti del web i loro testi per sole finalità illustrative didattiche e scientifiche.
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
Calore latente di fusione
Lo scopo principale di questa sezione è quello di provare come il calore ceduto a un corpo non sempre implichi un aumento di temperatura. L'eccezione è costituita dai cambiamenti di stato. Quando noi forniamo calore a un blocco di ghiaccio, la temperatura del ghiaccio aumenta fino ad arrivare a 0°C. Se forniamo ulteriore calore notiamo che la temperatura del ghiaccio non aumenta ma rimane costante. In questa fase infatti il calore fornito serve per far fondere il ghiaccio.
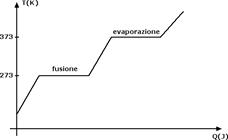 Quando tutto il ghiaccio è fuso, il calore che forniamo all'acqua serve di nuovo per aumentare la sua temperatura finché arriviamo a una temperatura di 100°C. A quel punto il calore ulteriore che cediamo serve al nuovo cambiamento di stato, da liquido a gas. In questa fase di nuovo la temperatura rimane costante finché tutta l'acqua non è evaporata. L'andamento della temperatura T in funzione del calore Q è riportato nel seguente grafico:
Quando tutto il ghiaccio è fuso, il calore che forniamo all'acqua serve di nuovo per aumentare la sua temperatura finché arriviamo a una temperatura di 100°C. A quel punto il calore ulteriore che cediamo serve al nuovo cambiamento di stato, da liquido a gas. In questa fase di nuovo la temperatura rimane costante finché tutta l'acqua non è evaporata. L'andamento della temperatura T in funzione del calore Q è riportato nel seguente grafico:
Dopo questa introduzione qualitativa cerchiamo di capire quanto calore serve per far fondere una massa m di ghiaccio o di una qualunque sostanza allo stato solido. È abbastanza intuitivo che questo calore risulta tanto maggiore quanto maggiore è la massa m di sostanza da fondere. In particolare, il calore di fusione Q e la massa m sono direttamente proporzionali Q = λf · m. Il coefficiente di proporzionalità prende il nome di calore latente di fusione e dipende dalla sostanza che prendiamo in esame. Dal momento che λf = Q / m la sua unità di misura nel Sistema Internazionale è il J / kg. Nel caso particolare dell'acqua abbiamo che λf = 3.34 · 105 J / kg. Questo significa che, a pressione atmosferica, per fondere 1 kg di ghiaccio servono 3.34 · 105 J.
È importante precisare a pressione atmosferica perché, se cambiamo la pressione, le grandezze fisiche che caratterizzano il cambiamento di stato cambiano. Ad esempio, se aumentiamo la pressione sul ghiaccio possiamo abbassare la temperatura di fusione al di sotto degli 0°C. Ci si può rendere conto di ciò mantenendo a qualche grado sotto lo zero un blocco di ghiaccio. Appoggiando sopra tale blocco un filo dotato alle sue estremità di due pesi, abbiamo che la pressione esercitata dal filo sul ghiaccio abbassa la temperatura di fusione e il ghiaccio sotto il filo comincia a fondere. Il filo riesce a penetrare nel blocco di ghiaccio mentre al di sopra del filo la pressione torna ad essere quella atmosferica e si ricrea il blocco di ghiaccio visto che siamo a una temperatura inferiore a 0°C. In questo modo il filo riesce ad attraversare completamente il blocco di ghiaccio!
Fonte: http://digilander.libero.it/quantum2008/APPUNTI/dispense%20di%20fisica%20II.doc
Autore del testo: non indicato nel documento di origine
Parola chiave google : Calore latente di fusione tipo file : doc
Visita la nostra pagina principale
Calore latente di fusione
Termini d' uso e privacy