Domande di fisica tecnica
Domande di fisica tecnica
Questo sito utilizza cookie, anche di terze parti. Se vuoi saperne di più leggi la nostra Cookie Policy. Scorrendo questa pagina o cliccando qualunque suo elemento acconsenti all’uso dei cookie.I testi seguenti sono di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente a studenti , docenti e agli utenti del web i loro testi per sole finalità illustrative didattiche e scientifiche.
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
Domande di fisica tecnica
- PRIMO PRINCIPIO DEI SISTEMI APERTI
- TH. BERNOULLI: SPIEGARE E DERIVARE CON IPOTESI
- ENTROPIA: DEFINIRE E RELAZIONE A SECONDO PRINCIPIO
- PRIMO PRINCIPIO TERMODINAMICA E ESPERIENZA JOULE
- SECONDO PRINCIPIO TERMODINAMICA
- POSTULATO DI FOURIER
- CONVEZIONE: DESCRIZIONE, LEGGE, TERMINI
- CONDUZIONE: DESCRIZIONE, LEGGE, TERMINI
- RESISTENZA TERMICA IN CONDUZIONE E CONVEZIONE
- LEGGE STEPHAN BOLTZMANN
DAGLI APPUNTI:
- LEGGE DI STEVINO
- PRINCIPIO ZERO DELLA TERMIDINAMICA
- TRASFORMAZIONE QUASISTATICA
- GAS IDEALE
- LEGGE DI MAYER
- KELVIN
- CLAUSIUS
- REVERSIBILITA’
- TEOREMA DI CARNOT
- LAVORO TECNICO
- IRRAGIAMENTO
- ENTALPIA
- PRIMO PRINCIPIO DEI SISTEMI APERTI
- TH. BERNOULLI: SPIEGARE E DERIVARE CON IPOTESI
![]()
in cui:
- v rappresenta la velocità del fluido lungo la linea di flusso,
- g è l'accelerazione di gravità,
- h è la quota altimetrica (ovvero l'altezza rispetto ad un riferimento orizzontale, di un qualsiasi punto all`interno del condotto),
- p rappresenta la pressione lungo la linea di flusso,
- ρ è la densità del fluido.
- ENTROPIA: DEFINIRE E RELAZIONE A SECONDO PRINCIPIO
- PRIMO PRINCIPIO TERMODINAMICA E ESPERIENZA JOULE
Il primo principio della termodinamica (anche detto, per estensione, legge di conservazione dell'energia) è un assunto fondamentale della teoria della termodinamica. Alla base del primo principio sta l'equivalenza tra calore e lavoro. Il primo principio è dunque un principio di conservazione dell'energia.
Tale equivalenza fu dimostrata da Joule attraverso un esperimento nel quale trasferiva energia meccanica al sistema tramite la caduta di un peso accoppiato meccanicamente ad un albero verticale tramite una corda che lo avvolge nella sua parte superiore mentre nella parte inferiore sono infisse delle pale immerse in un liquido contenuto in un recipiente adiabatico, Risultato dell'esperienza fu l'aumento della temperatura del liquido. Dimostrando così che l'energia di posizione del peso, in caduta frenata dal liquido che si opponeva alla sua variazione di quiete provocata dalla rotazione delle pale, si trasferiva in buona parte al liquido frenante aumentandone la temperatura, sviluppando un lavoro termico.
![]()
Nell'ipotesi di trasformazione quasi statica, ha senso parlare di variazione infinitesima quindi il primo principio può essere scritto in forma differenziale
![]()
Dove d è un differenziale esatto mentre, dato che le variazioni infinitesime di calore e lavoro esprimono differenziali non esatti, le indicheremo con il simbolo δQ e δL, infatti non sono funzioni di stato, in quanto dipendenti dal particolare percorso compiuto nel corso della trasformazione.
![]()
- SECONDO PRINCIPIO TERMODINAMICA
L'entropia di un sistema isolato lontano dall'equilibrio termico tende a salire nel tempo, finché l'equilibrio non è raggiunto. [Vedi Clausius, vedi Kelvin]
- POSTULATO DI FOURIER
(vedi appunti)
- CONVEZIONE: DESCRIZIONE, LEGGE, TERMINI
- CONDUZIONE: DESCRIZIONE, LEGGE, TERMINI
Per conduzione termica si intende la trasmissione di calore che avviene in un mezzo solido, liquido o gassoso dalle regioni a più alta temperatura verso quelle con temperatura minore per contatto molecolare diretto.
- RESISTENZA TERMICA IN CONDUZIONE E CONVEZIONE
La resistenza termica è un termine usato in fisica e particolarmente in elettronica per indicare la difficoltà del calore nell'attraversare un mezzo solido, liquido o gassoso. Essa dipende dalle specifiche costanti di conduzione e convezione e dalla geometria del mezzo.
- LEGGE STEPHAN BOLTZMANN
La legge di Stefan-Boltzmann, chiamata a volte legge di Boltzmann o anche legge di Stefan, stabilisce che la potenza irradiata da un corpo nero è proporzionale alla quarta potenza della sua temperatura: ![]()
dove U è l'energia irradiata dall'unità di superficie nell'unità di tempo (eccitanza), T la temperatura assoluta espressa in kelvin e σ è la costante di Stefan-Boltzmann che vale:
![]()
La legge, in questo enunciato, è valida solo per corpi neri ideali.
Per rendere conto della realtà nella legge di Stefan-Boltzmann si usa moltiplicare la costante σ per l'emissività ε, che dipende dalla superficie del corpo preso in considerazione oltre che dalla sua temperatura ed è compresa fra 0 (per i corpi idealmente bianchi) e 1 (per i corpi idealmente neri). Per cui per i corpi reali (chiamati anche "corpi grigi") si ha:
![]()
DAGLI APPUNTI:
- LEGGE DI STEVINO
Afferma che la pressione esercitata da una colonna di fluido di profondità h (distanza dal pelo libero del fluido, ossia la parte in alto nella colonnina aperta, a contatto con l'ambiente esterno) e densità costante ρ è direttamente proporzionale a h,
![]()
essendo l'accelerazione di gravità g = 9.8 m/s²; se la superficie della colonna di liquido è esposta alla pressione atmosferica PA allora la legge viene così modificata:
![]()
- PRINCIPIO ZERO DELLA TERMIDINAMICA
Il principio zero della termodinamica (detto talvolta zeresimo principio della termodinamica) stabilisce che, se un corpo A è in equilibrio termico con un corpo B, e se il corpo B è a sua volta in equilibrio termico con un altro corpo C, allora A è senz'altro in equilibrio termico con il corpo C
- TRASFORMAZIONE QUASISTATICA
Una trasformazione quasistatica è una trasformazione che avviene in modo estremamente lento, in maniera tale che il sistema in esame, passando dallo stato iniziale A a quello finale B, attraversa una successione di infiniti stati di equilibrio.
- GAS IDEALE
Un gas ideale è un modello ideale di gas che rispetta la legge dei gas perfetti:
![]()
in cui p è la pressione, V è il volume, n è il numero di moli, R è la costante dei gas perfetti (circa 8,314 J/K·mol) e T è la temperatura.
Per gas ideale si intende un gas che possieda le seguenti proprietà:
- le molecole sono puntiformi;
- interagiscono tra loro e con le pareti del recipiente mediante urti perfettamente elastici (ovvero non vi è dispersione di energia durante gli urti);
- non esistono forze di interazione a distanza tra le molecole del gas;
- le molecole del gas sono identiche tra loro e indistinguibili.
KELVIN
« è impossibile costruire una macchina ciclica che operi producendo lavoro a spese del calore sottratto a una sola sorgente»
- CLAUSIUS
« è impossibile realizzare una macchina ciclica che abbia come unico risultato il trasferimento di calore da un corpo freddo a uno caldo»
- REVERSIBILITA’
In termodinamica una trasformazione reversibile di un sistema termodinamico è una trasformazione che, dopo aver avuto luogo, può essere invertita riportando il sistema nelle condizioni iniziali senza che ciò comporti alcun cambiamento nel sistema stesso e nell'universo. In particolare, è richiesto che non avvenga dissipazione di energia. Una trasformazione per essere reversibile deve essere quasistatica, ovvero deve essere effettuata con delle variazioni infinitesime delle condizioni del sistema in modo che questo possa essere considerato in equilibrio termodinamico in ogni istante.
- TEOREMA DI CLAUSIUS
Il teorema di Clausius stabilisce un legame tra le quantità di calore scambiate da un sistema durante un ciclo e le temperature delle sorgenti che scambiano tale calore. Esso afferma che:
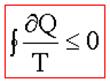
Se la trasformazione è reversibile l’integrale è pari a zero, altrimenti è minore se irreversibile.
- TEOREMA DI CARNOT
In termodinamica, il teorema di Carnot afferma che non è possibile realizzare una macchina termica operante tra due sorgenti che abbia un rendimento maggiore di quello della macchina di Carnot operante tra le stesse sorgenti.
Carnot dimostrò che la massima efficienza possibile di un qualsiasi motore ha un limite definito da η:
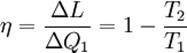
- IRRAGIAMENTO
L'irraggiamento è uno dei tre modi attraverso cui avviene la propagazione del calore. In particolare, al contrario della conduzione e della convezione, l'irraggiamento non prevede contatto diretto tra gli scambiatori, e non necessita di un mezzo per propagarsi.
Quindi è un fenomeno che interessa ogni aggregato materiale, non importa se solido, liquido o gassoso, e avviene anche nel vuoto. Questo è giustificato dal fatto che il trasferimento di calore per irraggiamento avviene sotto forma di onde elettromagnetiche.
- ENTALPIA
L'entalpia, solitamente indicata con H, è una funzione di stato che esprime la quantità di energia che un sistema termodinamico può scambiare con l'ambiente. L'entalpia è definita dalla somma dell'energia interna e del prodotto tra volume e pressione di un sistema. L'entalpia si misura in joule (SI, Sistema internazionale) o in calorie.
Fonte: http://www.unishare.it/files/313/Domande-fisica-tecnica11.doc
Sito web da visitare: http://www.unishare.it
Autore del testo: non indicato nel documento di origine
Nota : se siete l'autore del testo sopra indicato inviateci un e-mail con i vostri dati , dopo le opportune verifiche inseriremo i vostri dati o in base alla vostra eventuale richiesta rimuoveremo il testo.
Parola chiave google : Domande di fisica tecnica tipo file : doc
Domande di fisica tecnica
Visita la nostra pagina principale
Domande di fisica tecnica
Termini d' uso e privacy