Pressione atmosferica
Pressione atmosferica
Questo sito utilizza cookie, anche di terze parti. Se vuoi saperne di più leggi la nostra Cookie Policy. Scorrendo questa pagina o cliccando qualunque suo elemento acconsenti all’uso dei cookie.I testi seguenti sono di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente a studenti , docenti e agli utenti del web i loro testi per sole finalità illustrative didattiche e scientifiche.
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
Pressione atmosferica
La pressione atmosferica (ossia il rapporto fra il peso dell’aria e la superficie su cui essa agisce) al livello del mare, alla latitudine di 45° (accelerazione di gravità 9,8 m/sec2) e alla temperature di 0°C, fa equilibrio ad una colonnina verticale di mercurio alta 760 mm.
Questo valore corrisponde all’incirca a:
1033 g/cm2
1013 * 1000 dyn/cm2
1013 mb (1 mb = 1000 dyn/cm2)
1Pa = 1N/m2 = 10 dyn/cm2
1 hPa ( = 1000 dyn/cm2) = 1 mb (1Pa = 10 dyn/cm2)
1 atm = 760 mm Hg = 101 KPa
760 : 101 = X : 1; X = 7,5 1Kpa = 7,5 mm Hg
fonte: http://classequintaa.files.wordpress.com/2009/01/la-pressione-atmosferica.doc
Autore del testo: non indicato nel documento di origine
Pressione atmosferica
Come misurare la pressione atmosferica
Malgrado a Galileo mancasse la corretta interpretazione dell'effetto, a lui va comunque ascritto il merito della prima misura sperimentale della presunta "forza del vuoto". Egli effettuò la prova cercando quale fosse la forza minima necessaria per estrarre uno stantuffo a tenuta dall'incavo di un cilindro. L'esperimento è tecnicamente complesso e tutt'altro che facile da realizzare con le tecnologie del tempo, tanto che c'è chi insinua che Galileo 1'abbia soltanto immaginato, o magari tentato senza riuscire a portarlo a buon fine.
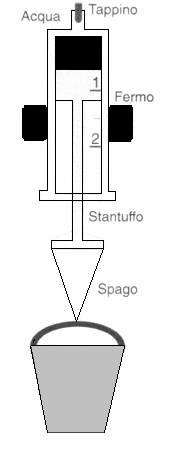 Oggi possiamo farlo a casa nostra in pochi minuti, arrivando a determinare con buona precisione il valore della pressione atmosferica. Ci si procuri una siringa farmaceutica "usa e getta", del tipo piccolo da 2,5 cc (millilitri), e se ne stimi la sezione interna. Per esempio, quella da me usata aveva i cc graduati con passo di 15,7 mm, il che denuncia una sezione di 0,637 cm2. Tolto 1'ago, si aspiri nella siringa un po' d'acqua, la si fissi in posizione verticale a punta in su e si elimini con cura ogni residuo d'aria, incluse le bollicine aderenti alle pareti (quando lo stantuffo verrà sottoposto a trazione, 1'aria potrebbe espandersi, rendendo meno facile la misura). Ora si otturi il foro superiore con un polpastrello, meglio ancora con un apposito tappino. Si leghi allo stantuffo uno spago e a esso si appenda un secchiello da spiaggia o altro recipiente leggero da circa un litro; è preferibile che la legatura sia fatta in modo simmetrico, così che il peso del secchiello agisca lungo 1'asse della siringa, senza produrre trazioni laterali, come suggerito nella figura. Ora si è pronti a operare. Con un bricco, si versino nel secchiello circa 600 g d'acqua (anche la sabbia va benissimo), poi si inizi ad aggiungerne dosi molto piccole, tenendo d'occhio lo stantuffo. Si arresti 1'operazione non appena si nota che quest'ultimo, inizialmente immobile, inizia a scivolare lentamente verso il basso (osservazione facilitata dalla graduazione presente sulla siringa). Questo ci dice che il peso di tutto 1'insieme, stantuffo più spago più secchiello più acqua, ha appena superato quello dell'aria atmosferica che preme sulla sezione dello stantuffo, accresciuto della forza d'attrito. Si misuri il peso del secchiello con 1'acqua per mezzo di una normale bilancia elettronica. La pressione atmosferica si ottiene, in prima approssimazione, dividendo questo dato per la sezione dello stantuffo. Se si usa una siringa di sezione più grande, il peso trovato sarà proporzionalmente maggiore. Per una misura più precisa, occorre mettere fuori gioco la forza d'attrito. Ciò si fa ripetendo tutto il ciclo di operazioni, pesatura inclusa, con la siringa stappata. Per far scendere lo stantuffo basterà adesso un peso molto minore, giacché 1'unica forza da vincere è quella dell'attrito. il dato che ci serve, quello che infine va diviso per la sezione, è la differenza tra i pesi misurati la prima e la seconda volta.
Oggi possiamo farlo a casa nostra in pochi minuti, arrivando a determinare con buona precisione il valore della pressione atmosferica. Ci si procuri una siringa farmaceutica "usa e getta", del tipo piccolo da 2,5 cc (millilitri), e se ne stimi la sezione interna. Per esempio, quella da me usata aveva i cc graduati con passo di 15,7 mm, il che denuncia una sezione di 0,637 cm2. Tolto 1'ago, si aspiri nella siringa un po' d'acqua, la si fissi in posizione verticale a punta in su e si elimini con cura ogni residuo d'aria, incluse le bollicine aderenti alle pareti (quando lo stantuffo verrà sottoposto a trazione, 1'aria potrebbe espandersi, rendendo meno facile la misura). Ora si otturi il foro superiore con un polpastrello, meglio ancora con un apposito tappino. Si leghi allo stantuffo uno spago e a esso si appenda un secchiello da spiaggia o altro recipiente leggero da circa un litro; è preferibile che la legatura sia fatta in modo simmetrico, così che il peso del secchiello agisca lungo 1'asse della siringa, senza produrre trazioni laterali, come suggerito nella figura. Ora si è pronti a operare. Con un bricco, si versino nel secchiello circa 600 g d'acqua (anche la sabbia va benissimo), poi si inizi ad aggiungerne dosi molto piccole, tenendo d'occhio lo stantuffo. Si arresti 1'operazione non appena si nota che quest'ultimo, inizialmente immobile, inizia a scivolare lentamente verso il basso (osservazione facilitata dalla graduazione presente sulla siringa). Questo ci dice che il peso di tutto 1'insieme, stantuffo più spago più secchiello più acqua, ha appena superato quello dell'aria atmosferica che preme sulla sezione dello stantuffo, accresciuto della forza d'attrito. Si misuri il peso del secchiello con 1'acqua per mezzo di una normale bilancia elettronica. La pressione atmosferica si ottiene, in prima approssimazione, dividendo questo dato per la sezione dello stantuffo. Se si usa una siringa di sezione più grande, il peso trovato sarà proporzionalmente maggiore. Per una misura più precisa, occorre mettere fuori gioco la forza d'attrito. Ciò si fa ripetendo tutto il ciclo di operazioni, pesatura inclusa, con la siringa stappata. Per far scendere lo stantuffo basterà adesso un peso molto minore, giacché 1'unica forza da vincere è quella dell'attrito. il dato che ci serve, quello che infine va diviso per la sezione, è la differenza tra i pesi misurati la prima e la seconda volta.
(Andrea Frova, LA FISICA SOTTO IL NASO)
http://www.itgdelai.it/alunni/turco/PAtmosferica.doc
MANOMETRI: MISURA DELLA PRESSIONE
L'atmosfera terrestre è costituita da una miscela di gas, in gran parte azoto (78,08%), ossigeno (20,95%), argo (0,9%), biossido di carbonio (0,03%). È presente anche vapor d'acqua in quantità che dipende dalle condizioni atmosferiche. In molte zone sono presenti anche componenti inquinanti. Lo strato di gas che costituisce l'atmosfera è più denso in prossimità della superficie terrestre che a maggiori altezze, in gran parte in conseguenza dell'attrazione gravitazionale. I costituenti gassosi dell'aria esercitano su tutti gli oggetti immersi nell'atmosfera terrestre una pressione provocata dal peso che gli oggetti subiscono ad opera degli atomi e delle molecole contenuti nell'aria sopra di essi.
IL BAROMETRO
Il metodo più usato per misurare la pressione atmosferica utilizza un apparecchio che prende il nome di barometro. Il barometro è stato inventato da Torricelli nel diciassettesimo secolo. È fatto di un tubo di vetro, chiuso a un'estremità, riempito di mercurio e poi capovolto in un altro contenitore di mercurio cosicché l'estremità aperta del tubo si trovi al di sotto della superficie del metallo. In questo modo il livello del mercurio nel tubo chiuso scende perché la forza di gravità attrae la colonna di mercurio in basso. Si ricordi che pressione = δHggh = (densità del mercurio)(accelerazione di gravità)(altezza) .
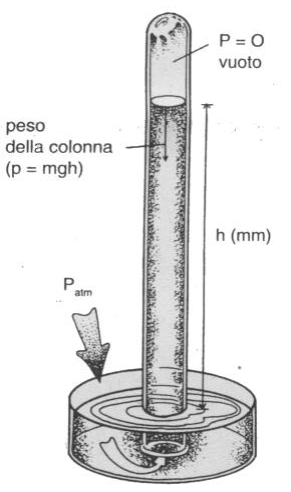
Figura 1: Barometro
Il tubo di mercurio non si vuota completamente perché ad un certo punto la pressione della colonna di mercurio (forza diretta verso il basso) è bilanciato dalla pressione che l'atmosfera esercita sulla superficie del mercurio nel recipiente sottostante. Questa pressione è trasmessa dal liquido e spinge verso l'alto la colonna che di per se stessa tenderebbe a scendere. Lo spazio vuoto alla sommità della colonna non contiene aria: in esso vi è il vuoto e la pressione è zero. L'unica pressione diretta verso il basso è quella dovuta al peso della colonna di mercurio (cioè δHggh) e, come mostrato nella Figura 1, è bilanciata dalla forza dovuta alla pressione atmosferica. Perciò l'altezza della colonna è direttamente proporzionale alla pressione esercitata dall'atmosfera.
L'altezza del mercurio nel barometro varia sia con l'altezza sul livello del mare (diminuisce alle grandi altezze dove l'aria è meno densa) sia con le condizioni atmosferiche. In condizioni normali e a livello del mare la pressione che esercitano i gas atmosferici sostiene una colonna di mercurio dell'altezza di 760 mm. Ne consegue che una atmosfera corrisponde, per definizione, a 760 mmHg ossia a 760 Torr (1 mmHg = 1 Torr), unità così chiamata in onore di Torricelli.
IL MANOMETRO A TUBO APERTO
Per misurare la pressione di un campione di gas si utilizza un manometro, cioè un misuratore di pressione. Vi sono due tipi fondamentali di manometro, quello a tubo aperto e quello a tubo chiuso. Del manometro a tubo chiuso non parleremo. Un manometro a tubo aperto è essenzialmente un tubo curvato a U e riempito di mercurio. Un estremo è aperto e collegato con l'atmosfera (da qui la denominazione di tubo aperto), mentre l'altro estremo è collegato a un recipiente o a un pallone riempito di gas che presenta una pressione superiore o inferiore a quella esercitata dall'atmosfera.
Nella Figura 2 la pressione atmosferica sostiene la colonna nel braccio destro del tubo a U, mentre la pressione del gas nel pallone sostiene la colonna contenuta nel braccio sinistro. La colonna di sinistra è più alta della colonna di destra esattamente della differenza di pressione tra il gas e l'atmosfera: δHggΔh = (Pgas - Patm). La pressione atmosferica si ricava leggendo un barometro. La pressione del gas Pgas viene così calcolata: Pgas = Patm + δHggΔh. Ne consegue che la pressione. del gas è maggiore della pressione atmosferica della quantità δHggΔh. Invece se la pressione del pallone fosse inferiore a quella atmosferica la colonna di destra sarebbe più alta di quella di sinistra. In questo caso al pressione del gas nel pallone è: Pgas = Patm -δHggΔh.
Un tipo semplice di manometro a tubo aperto è mostrato nella Figura 3. Si tratta semplicemente di un tubo di vetro a forma di U montato su una tavoletta di legno sulla quale è fissata una scala graduata per misurare il valore di Δh. Con questo dispositivo è possibile misurare la pressione di un campione di gas (che viene attaccato “al vuoto” di Figura 3) che abbia una pressione propria sia maggiore che inferiore a quella atmosferica addizionando o sottraendo Δh dalla pressione barometrica nota.
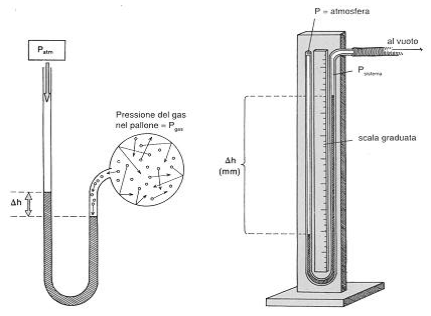
Figura 2 Manometro a tubo aperto Figura 3
(DAL SITO: www.chimicando.it)
fonte: http://www.liceoagnoletti.it/attivita/attivita_professori/fisicafacile/Documenti/IIA_BAROMETRI%20e%20MANOMETRI.doc
Autore del testo: non indicato nel documento di origine
Pressione atmosferica
Visita la nostra pagina principale
Pressione atmosferica
Termini d' uso e privacy