Metodo semplificato per il calcolo del pH di acidi o basi deboli
Metodo semplificato per il calcolo del pH di acidi o basi deboli
Questo sito utilizza cookie, anche di terze parti. Se vuoi saperne di più leggi la nostra Cookie Policy. Scorrendo questa pagina o cliccando qualunque suo elemento acconsenti all’uso dei cookie.I testi seguenti sono di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente a studenti , docenti e agli utenti del web i loro testi per sole finalità illustrative didattiche e scientifiche.
![]()
Metodo semplificato per il calcolo del pH di acidi o basi deboli
In certi casi è possibile calcolare la concentrazione di equilibrio degli ioni H+, ricorrendo a delle approssimazioni che consentono di non dover risolvere le equazioni di equilibrio.
E' possibile ricorrere a tali semplificazioni quando possiamo ragionevolmente ritenere che la concentrazione di equilibrio degli ioni H+ sia molto minore della concentrazione iniziale dell'acido. Ciò accade quando il grado di dissociazione dell'acido assume valori bassi. Affinchè tali condizioni si verifichino è necessario che l'acido sia debole (ka bassa) e che la soluzione non sia eccessivamente diluita (se è molto diluita aumenta infatti il grado di dissociazione.
In linea di massima possiamo applicare tale metodo quando il valore della ka è minore del valore della concentrazione iniziale di almeno tre ordini di grandezza.
Prendendo in considerazione il solito acido debole generico HA, l'equilibrio di dissociazione è
HA H+ + A-
e la costante di equilibrio vale
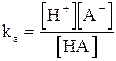
Se poniamo pari ad X il numero di mol/l di HA che si dissociano, possiamo costruire la seguente tabella delle concentrazioni iniziali e delle concentrazioni di equilibrio
|
iniziale |
d'equilibrio |
[HA]
|
Ciniz
|
Ciniz - X
|
[H+]
|
0
|
X
|
[A-]
|
0
|
X
|
Poniamo ora, come al solito, le concentrazioni di equilibrio, espresse in funzione di X, in relazione con la ka
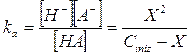
Ora, se, come abbiamo ipotizzato, X << Ciniz, è possibile trascurare la X nella differenza a denominatore. La relazione diventa allora
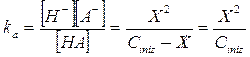
Dalla quale otteniamo la seguente relazione semplificata, per il calcolo della concentrazione di equilibrio degli ioni H+
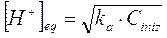
Fonte: http://digidownload.libero.it/quintaachimica/CHIMICA.doc
Autore del testo: non indicato nel documento di origine
Parola chiave google : Metodo semplificato per il calcolo del pH di acidi o basi deboli tipo file : doc
Metodo semplificato per il calcolo del pH di acidi o basi deboli
![]()
Se vuoi trovare velocemente le pagine inerenti un determinato argomento come Metodo semplificato per il calcolo del pH di acidi o basi deboli utilizza il seguente motore di ricerca :
Visita la nostra pagina principale
Metodo semplificato per il calcolo del pH di acidi o basi deboli
Termini d' uso e privacy